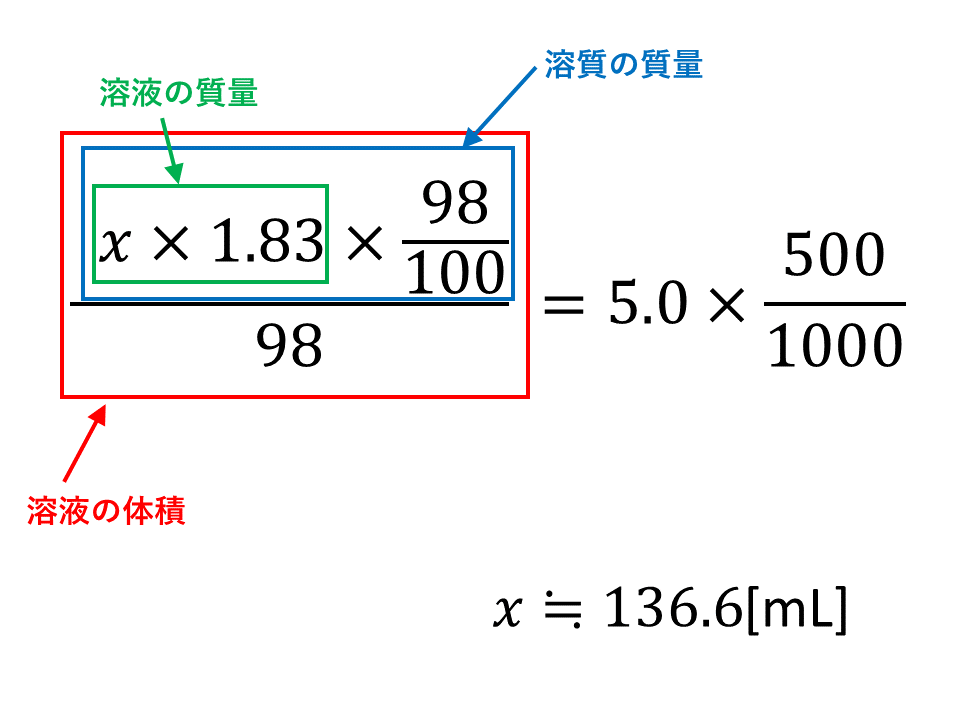
=(食塩水)×01 (食塩水)に01をかけるとになるのだから、(食塩水)は0とすぐに分かる方は、以下の計算する必要はありません。 (食塩水)=÷01 =0g ここで、食塩水が0gと出ましたが、この問題では、水の量を出したいので、食塩の分gを
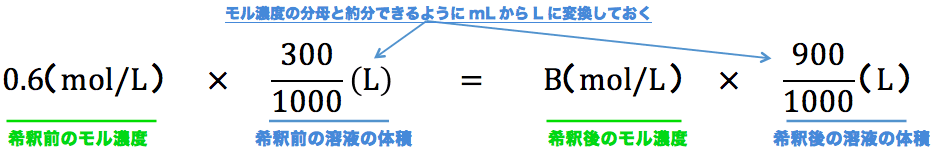
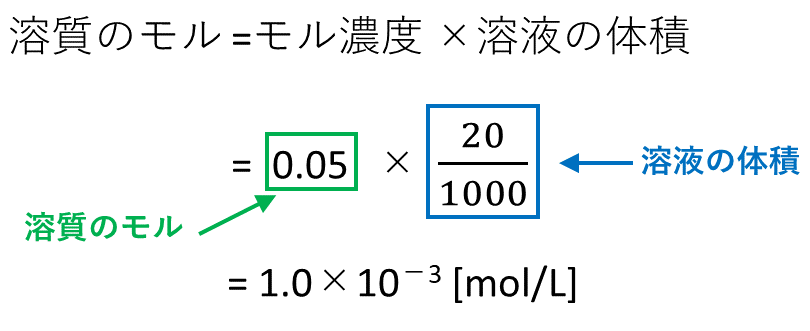
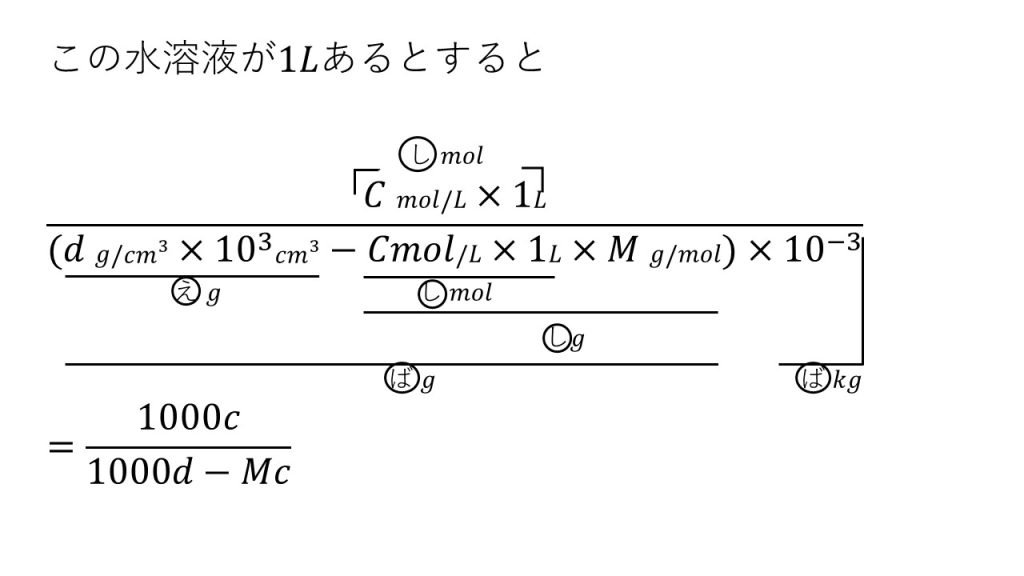
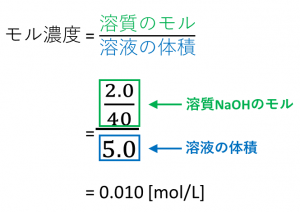
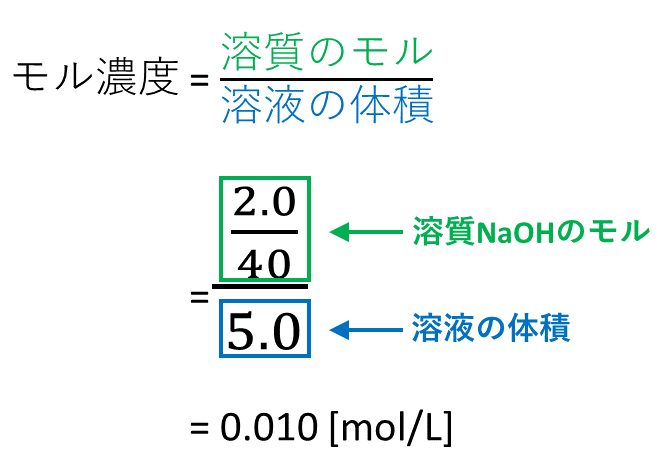
水溶液 濃度 求め方- 溶質の物質量 mol / 溶液の体積 L で計算できるので、 求めるモル濃度は 05 mol / 2 L = 025 mol/L・・・(答) となります。 モル濃度は、溶質の物質量 mol / 溶液の体積 Lで求める溶液の濃度を \(x\) (%)とすると \( 100\times \displaystyle \frac{160}{250}=()\times \displaystyle \frac{x}{100}\) これを解いて \( x\,=\,128\) (%)
水溶液 濃度 求め方のギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 | 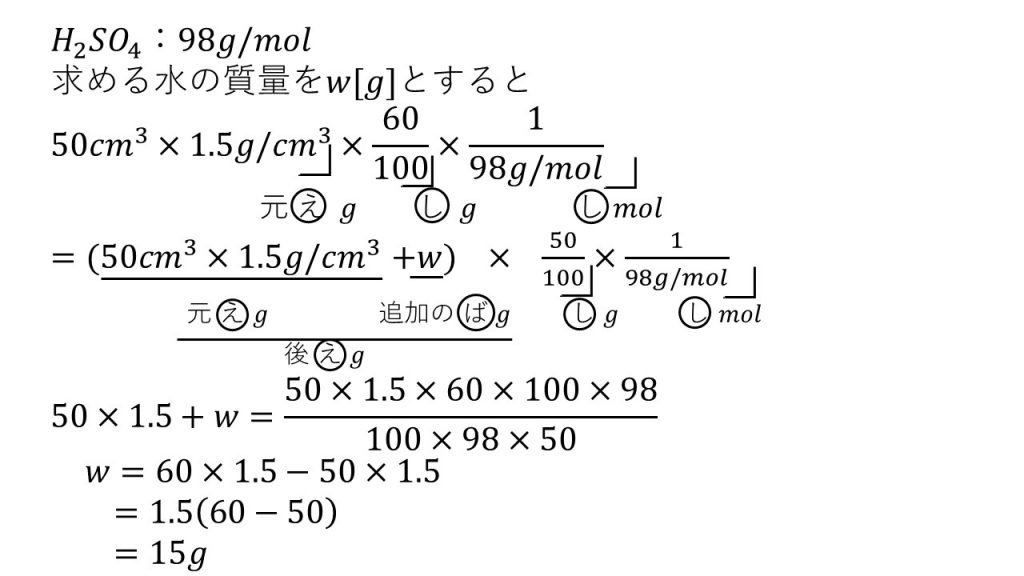 |  |
 |  |  |
 |  | |
 |  |  |
「水溶液 濃度 求め方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
 |  |  |
「水溶液 濃度 求め方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 |  |  |
 |  | |
「水溶液 濃度 求め方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
 | ||
 |  |  |
「水溶液 濃度 求め方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  | |
 |  |  |
「水溶液 濃度 求め方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 |  |  |
 |  | |
「水溶液 濃度 求め方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  |  |
「水溶液 濃度 求め方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
 |
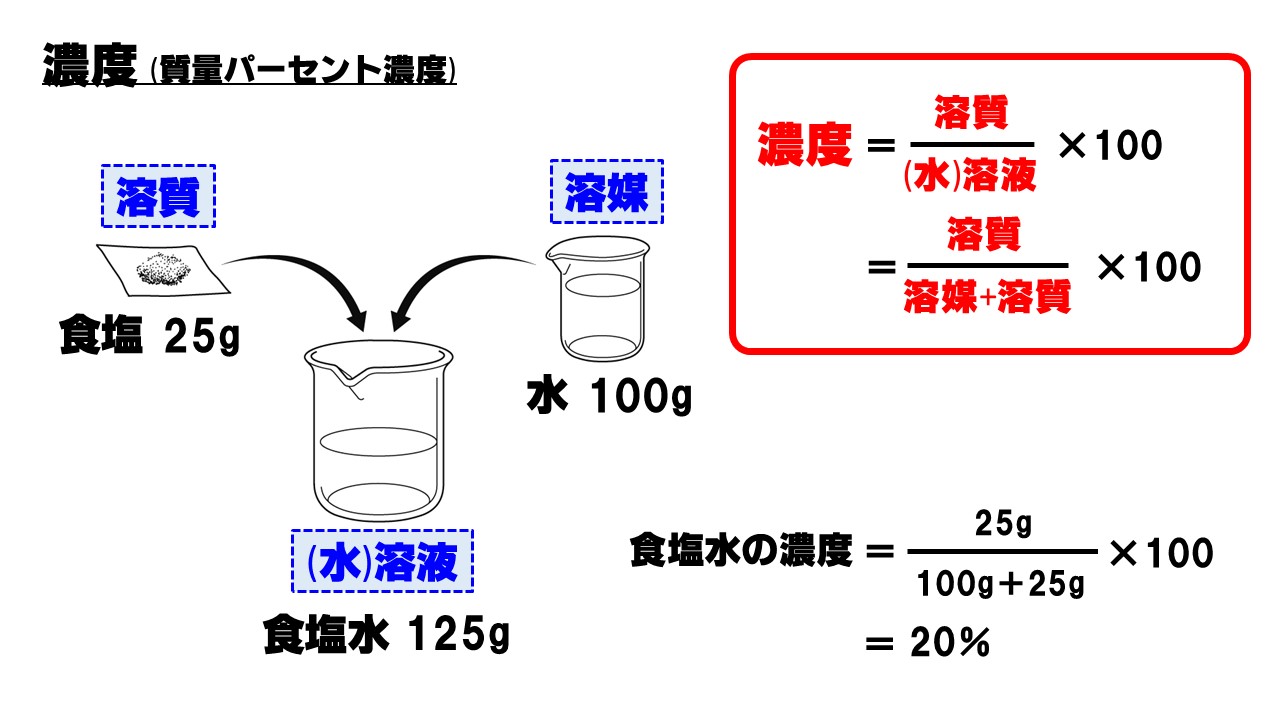
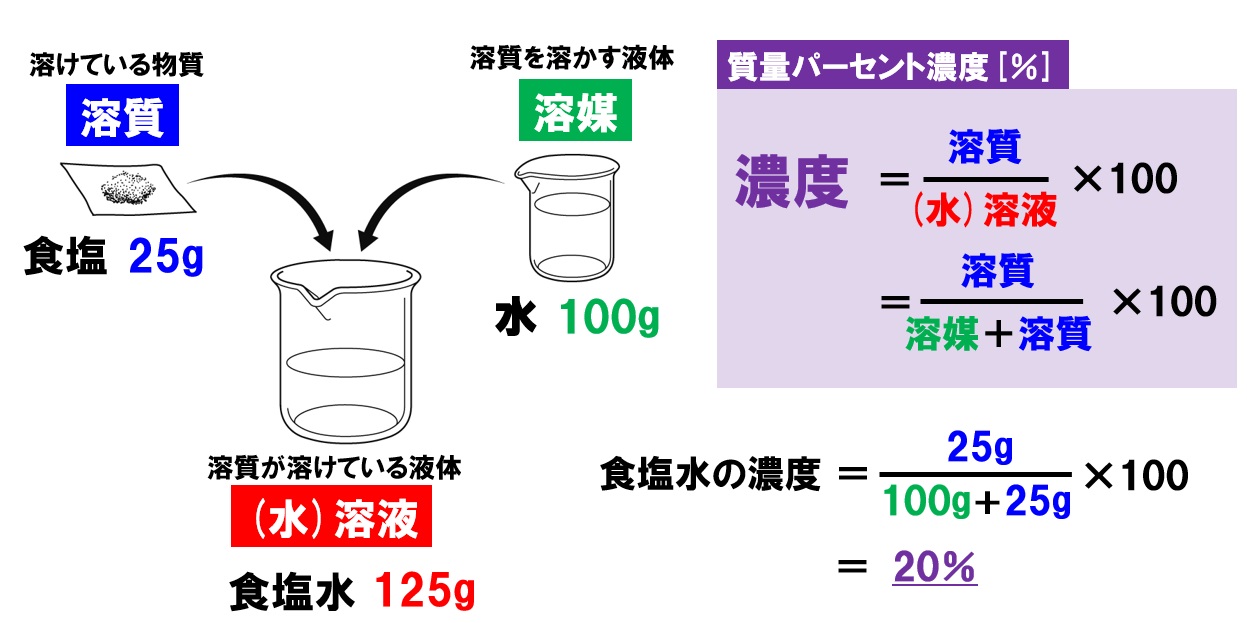
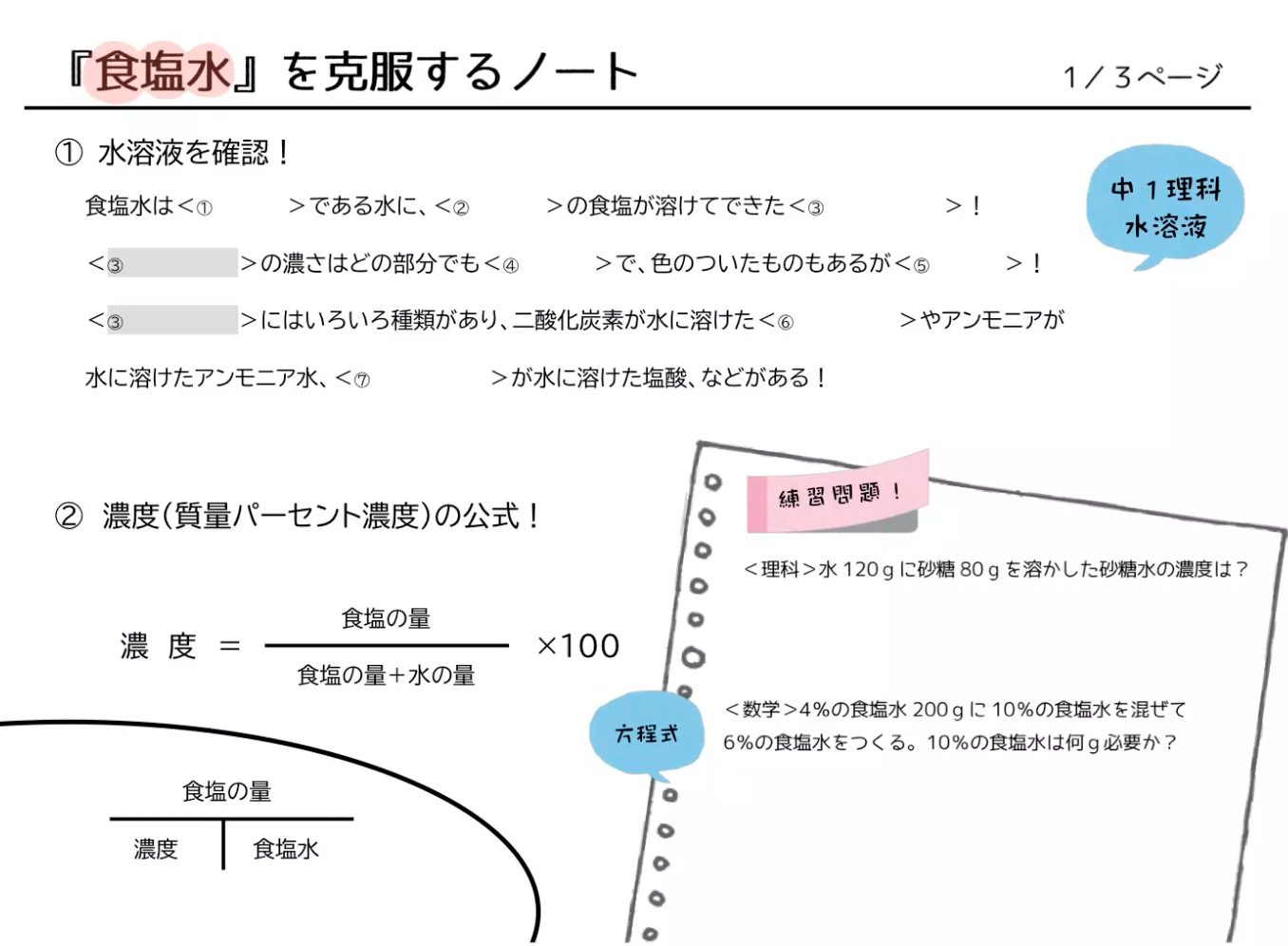
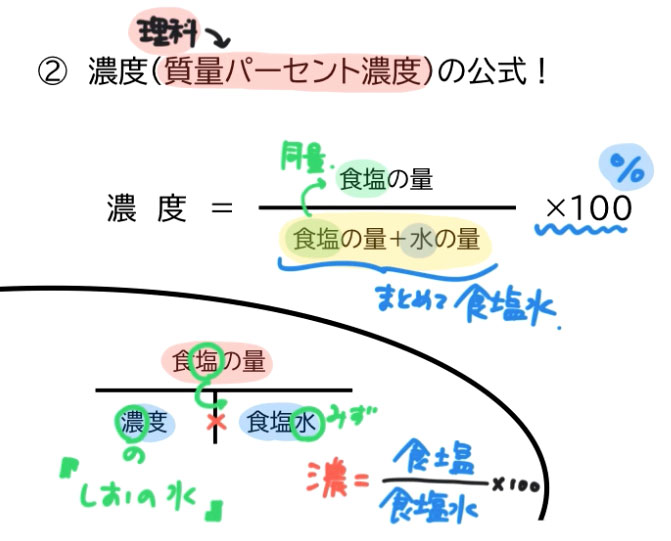
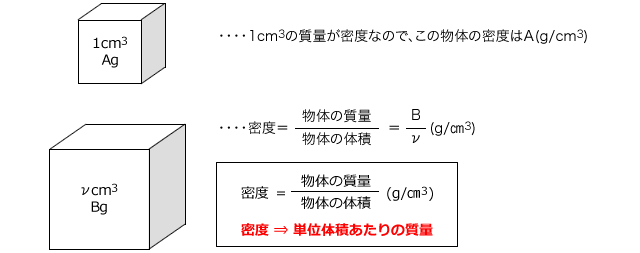
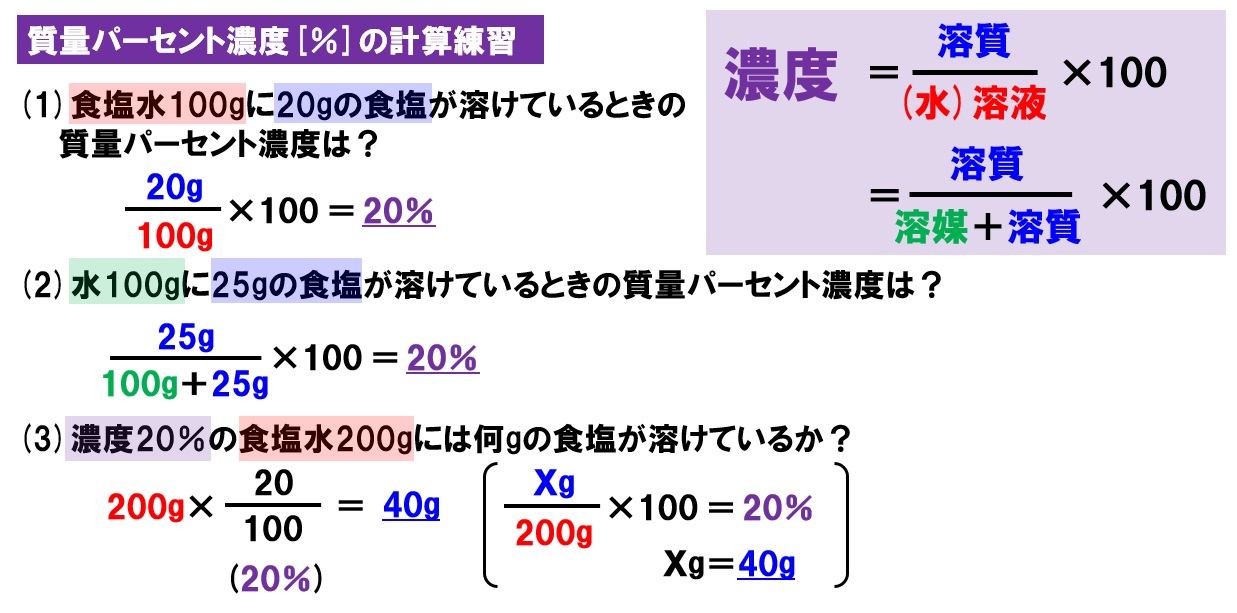
では、質量パーセント濃度はどうやって求めるのでしょうか? 先ほども言いましたが質量パーセント濃度は「 ある溶液中に溶けている溶質の割合 」です。 つまり、溶質の質量が溶液の6年弱前 溶液の質量は、溶質の質量 + 溶媒の質量 溶質の質量は、溶液の質量×質量パーセント濃度÷100 溶媒の質
Incoming Term: 水溶液 濃度 求め方,




0 件のコメント:
コメントを投稿